Imagina sentir un alivio real del dolor con solo creer que un tratamiento funciona. Ese es el poder del efecto placebo: una respuesta fisiológica que no depende de la acción directa de un fármaco, sino de la expectativa de mejora. Durante décadas, los científicos han observado este fenómeno en pacientes, sin embargo, hasta ahora se desconocía con precisión cómo se activa ese sistema, qué neuronas están implicadas o qué ocurre exactamente dentro del cerebro. Entender cómo el cerebro genera este alivio es clave para mejorar los tratamientos del dolor crónico.
Un equipo de investigadores del centro RIKEN en Japón logró descifrar los engranajes biológicos del placebo en un modelo animal de dolor neuropático. El estudio, publicado en Science Advances, muestra que la activación de señales opioides en la corteza prefrontal medial (mPFC) desencadena una cascada que termina inhibiendo la percepción del dolor a través del sistema descendente de modulación. Esta vía, que conecta directamente con el tronco encefálico, se activa al recibir una “orden” de alivio generada por la expectativa aprendida.
Este avance fue posible gracias al uso de herramientas genéticas y optogenéticas en ratas modificadas. Mediante condicionar a los animales con un analgésico real y luego sustituirlo por placebo, los investigadores identificaron cambios neuronales específicos, incluyendo la inhibición de ciertas neuronas GABAérgicas y la activación de vías que bloquean la transmisión del dolor. El hallazgo podría allanar el camino para terapias que refuercen el placebo en entornos clínicos reales.
“Muchos investigadores no creían que los animales pudieran experimentar el efecto placebo”, dijo Yilong Cui del Centro RIKEN de Ciencias Médicas Integrativas. “Pero logramos inducirlo en roedores usando el acondicionamiento pavloviano”.
Una corteza clave: el papel de la región prefrontal medial
La corteza prefrontal medial (mPFC) es una región cerebral vinculada con funciones ejecutivas, toma de decisiones y modulación emocional. En este estudio, se descubrió que también actúa como un centro de control que puede iniciar la inhibición del dolor cuando se activa por señales opioides endógenas. Esta activación se produce sin necesidad de medicamentos, desencadenada por la expectativa de alivio generada por el condicionamiento.
Los investigadores identificaron un tipo específico de neuronas en esta región: las MOR+ (que expresan receptores μ-opioides). Estas neuronas resultaron fundamentales para bloquear la respuesta al placebo cuando fueron activadas artificialmente, y para permitirla cuando fueron inhibidas.
El estudio demostró que las MOR+ inhiben otras neuronas excitatorias que se proyectan hacia una zona profunda del cerebro conocida como el gris periacueductal ventrolateral (vlPAG), que coordina la respuesta analgésica descendente.
Este circuito cortico-subcortical no solo es específico sino también altamente selectivo. Las MOR+ actúan como un “freno” natural sobre las señales que pueden aliviar el dolor. Al desactivar ese freno mediante la acción de opioides endógenos inducidos por el placebo, el sistema descendente queda liberado y empieza a inhibir activamente la percepción del dolor. Este mecanismo explica por qué el placebo puede tener efectos fisiológicos tangibles.
Condicionamiento clásico: así se induce el efecto placebo
Para inducir el efecto placebo en los animales, los investigadores usaron una estrategia de condicionamiento similar a la utilizada en humanos. Durante cuatro días consecutivos, se inyectó un analgésico real (gabapentina) a las ratas, que aprendieron a asociar la inyección con alivio. En el quinto día, se sustituyó el fármaco por una inyección salina inerte.
Sorprendentemente, muchas ratas mostraron una disminución en la percepción del dolor, lo que confirma que el cerebro había aprendido a responder al estímulo.
No todas las ratas respondieron igual. Alrededor de un tercio mostró una respuesta placebo completa, otro tercio una respuesta parcial, y el resto no respondió. Esta variabilidad refleja lo que también ocurre en humanos y abre la puerta a estudiar por qué algunas personas son más sensibles al placebo que otras, posiblemente por diferencias en la conectividad o expresión de receptores cerebrales.
Lo más interesante es que, al manipular específicamente la actividad de las neuronas MOR+ en la mPFC, los investigadores lograron bloquear por completo la respuesta placebo. Esto confirma que este tipo de neuronas no solo está implicado, sino que es esencial para que el cerebro pueda traducir una expectativa en una respuesta real de alivio del dolor.
Un circuito descendente que bloquea el dolor
El efecto placebo no actúa directamente sobre la zona donde duele, sino que activa un circuito descendente que comienza en la corteza y termina en el tronco encefálico.
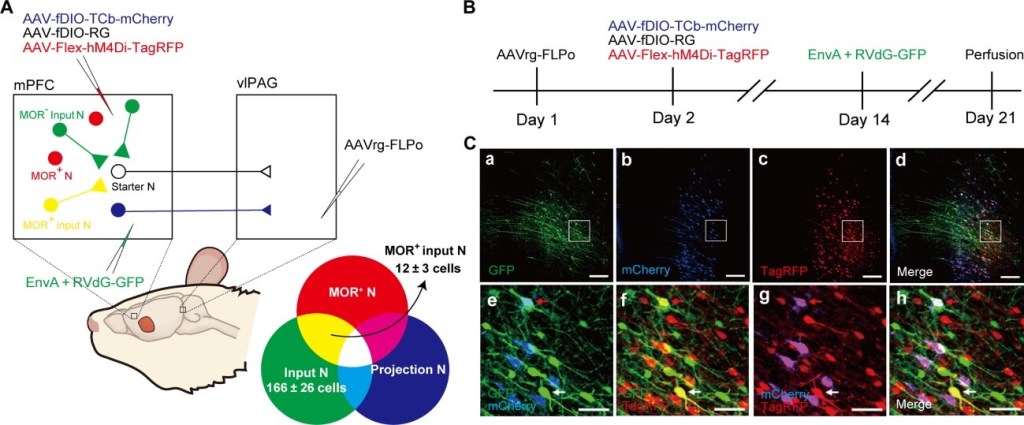
En este estudio, se identificó con precisión que la vía va desde las neuronas piramidales de la capa V de la mPFC hacia el área ventrolateral del gris periacueductal (vlPAG). Esta estructura es clave en la inhibición de señales dolorosas antes de que lleguen a la corteza sensorial.
Usando técnicas de trazado anterógrado y retrógrado, el equipo demostró que estas neuronas forman conexiones monosinápticas. Además, mediante registros electrofisiológicos y optogenética, comprobaron que las MOR+ inhiben directamente las neuronas que proyectan hacia el vlPAG mediante receptores GABAA. Esta desinhibición permite que la información excitatoria fluya hacia abajo y active el sistema inhibitorio del dolor.
Cuando se interrumpió este circuito específico, el efecto placebo desapareció, incluso si las neuronas MOR+ estaban funcionando. Esto demuestra que el alivio del dolor por placebo depende no solo de la activación en la mPFC, sino también de la integridad funcional del trayecto hacia el vlPAG. Este hallazgo refuerza la importancia del sistema descendente como modulador activo del dolor.
Implicaciones para el tratamiento del dolor crónico
La posibilidad de inducir una respuesta analgésica sin fármacos abre una vía prometedora para reducir el uso de opioides, especialmente en casos de dolor crónico.
Los resultados de este estudio sugieren que es posible potenciar mecanismos internos del cerebro mediante técnicas conductuales como el condicionamiento o la terapia psicológica. Si se logra activar el circuito mPFC-vlPAG en humanos, podría desarrollarse una medicina más personalizada y con menos efectos secundarios.
El hallazgo también podría explicar por qué algunas personas responden mejor a ciertos tratamientos, aunque estos no tengan ingredientes activos potentes. Comprender las bases neurobiológicas del placebo permitiría predecir qué pacientes tienen mayor probabilidad de beneficiarse de terapias basadas en expectativa y aprendizaje.
Esto no significa sustituir fármacos por placebo, sino aprender a integrar esta capacidad natural del cerebro como complemento terapéutico.
En el futuro, podría emplearse incluso en enfermedades más allá del dolor, como depresión o insomnio, donde también intervienen circuitos de expectativa y recompensa.
Expectativa, aprendizaje y analgesia: un nuevo paradigma
El estudio también contribuye a entender las diferencias entre placebo dependiente de la expectativa consciente y el inducido por condicionamiento clásico. En este caso, la analgesia surgida en ratas con dolor neuropático sugiere que el aprendizaje por repetición de un estímulo es suficiente para activar el sistema opioide endógeno, incluso sin una expectativa consciente.
Esto apunta a que el placebo no es solo un efecto mental subjetivo, sino una reacción neurobiológica que puede programarse mediante experiencias repetidas.
La asociación entre inyección y alivio se graba en la red neuronal y puede reactivarse con un estímulo similar, aunque sea inerte. Es un aprendizaje profundo, no necesariamente verbalizado.
A la luz de estos resultados, el placebo se revela como un proceso activo y no como una ilusión. El cerebro genera su propia farmacia interna y la libera en respuesta a claves específicas. Saber cómo funciona ese “botón interno del analgésico” podría transformar la forma en que comprendemos la relación entre mente, cuerpo y medicina.
Aprovechar el placebo para curar
Este estudio es el primero en demostrar con detalle cómo funciona el efecto placebo en animales con dolor crónico, usando herramientas de neurociencia moderna.
Al identificar las neuronas MOR+ y su conexión directa con el sistema descendente de inhibición del dolor, los investigadores han abierto una vía para traducir este conocimiento en estrategias clínicas que mejoren la eficacia de los tratamientos.
El efecto placebo no es una falsedad ni una casualidad, sino una capacidad biológica que el cerebro tiene para autorregular el dolor. Potenciarlo podría significar menos dependencia de opioides, menos efectos secundarios y mayor calidad de vida para pacientes con enfermedades crónicas. En un mundo con una crisis global de sobredosis, esta alternativa cobra un valor incalculable.
Comprender y aprovechar el placebo significa también apostar por una medicina que reconoce el poder de la mente y el aprendizaje en la sanación del cuerpo. Y ese puede ser el primer paso hacia terapias más humanas, integradoras y eficaces.
Referencias
- Hiroyuki Neyama et al. Opioidergic activation of the descending pain inhibitory system underlies placebo analgesia.Sci. (2025).DOI:10.1126/sciadv.adp8494
Cortesía de Muy Interesante
Dejanos un comentario: