¿Hay algo que te contaron como imposible cuando estabas en el instituto? Correcto: ver moverse a un electrón en plena acción química podría parecer más propio de una fantasía de ciencia ficción que de un logro real. Sin embargo, eso es exactamente lo que ha conseguido un equipo internacional de investigadores, es decir, capturar por primera vez la reconfiguración espacial de un electrón durante una reacción química real. Un paso que, hasta ahora, era tan deseado como inalcanzable. Otra pantalla pasada en el juego de la física cuántica.
Para lograrlo, fue necesaria una combinación precisa de condiciones. El experimento se realizó sobre moléculas de amoníaco sometidas a un disparo ultrarrápido de rayos X, en un entorno que permitió ver, literalmente, cómo un único electrón de valencia —los que participan en los enlaces químicos— se reorganizaba al romperse una molécula. Según los autores, esta observación abre nuevas vías para controlar y entender mejor los mecanismos que están en el corazón mismo de la química y la biología molecular.
Una fotografía de lo que nunca se había visto
Uno de los principales obstáculos a la hora de observar electrones en movimiento es que los métodos clásicos de dispersión de rayos X tienden a registrar sobre todo el comportamiento de los electrones internos, los más cercanos al núcleo atómico. Son los electrones de valencia, en cambio, los que participan activamente en las reacciones químicas, pero su señal es débil y fácil de perder entre los datos.
El equipo dirigido por Ian Gabalski, del Stanford PULSE Institute, encontró una solución ingeniosa. Eligieron trabajar con ND₃, una forma isotópica del amoníaco en la que los átomos de hidrógeno son reemplazados por deuterio; este cambio aumenta la masa de la molécula, lo que ayuda a distinguir mejor el movimiento electrónico del movimiento nuclear durante la reacción. Eso reduce la interferencia de electrones centrales y aumenta la posibilidad de detectar el tenue rastro de un electrón periférico al cambiar de estado.
La clave del experimento fue excitar la molécula con un pulso ultravioleta que promoviera uno de sus electrones a un orbital de Rydberg, un nivel energético alto y transitorio. Acto seguido, un disparo de rayos X de 10 keV captó cómo evolucionaba la nube de densidad electrónica durante los primeros 600 femtosegundos (una fracción ínfima de segundo) de la reacción.
¿Qué significa “ver” un electrón en movimiento?
“Ver” un electrón no implica observarlo con luz visible ni a través de un microscopio convencional, porque estos instrumentos utilizan longitudes de onda mucho mayores que las escalas subatómicas. Los electrones son partículas extremadamente pequeñas —de hecho, no tienen tamaño definido en el sentido clásico— y su comportamiento está regido por las leyes de la mecánica cuántica, donde no se habla de trayectorias concretas, sino de probabilidades de presencia en distintas regiones del espacio.
Cuando los científicos dicen que han “visto” un electrón en movimiento, se refieren a que han sido capaces de registrar experimentalmente cómo cambia su distribución de densidad en el tiempo. Es decir, han medido cómo evoluciona la forma y posición de su nube de probabilidad, una región del espacio donde es más o menos probable encontrar al electrón.
Como se ha comentado, en este estudio no se utilizó luz visible, sino rayos X ultrarrápidos, con longitudes de onda lo suficientemente pequeñas como para interactuar con estructuras atómicas. Al analizar cómo esos rayos X se dispersan al atravesar la nube electrónica de una molécula excitada, los científicos pueden reconstruir una imagen indirecta pero precisa del estado del electrón en distintos momentos de la reacción. Esa “imagen” no es una fotografía, sino una representación basada en patrones de interferencia de los rayos X, combinados con simulaciones cuánticas avanzadas.
En resumen, “ver” un electrón significa mapear su presencia a través de su impacto en otros fenómenos físicos que sí podemos medir, como la dispersión de partículas. Es un logro técnico extraordinario que nos permite observar lo invisible con herramientas creadas para descifrar lo más profundo de la materia.
Un electrón en pleno salto cuántico
Como indican los autores del estudio, el experimento permitió visualizar directamente el cambio en la distribución espacial del electrón de valencia. “Observamos las firmas de la reorganización electrónica de valencia en el amoníaco fotoexcitado mediante dispersión de rayos X duros ultrarrápidos” .
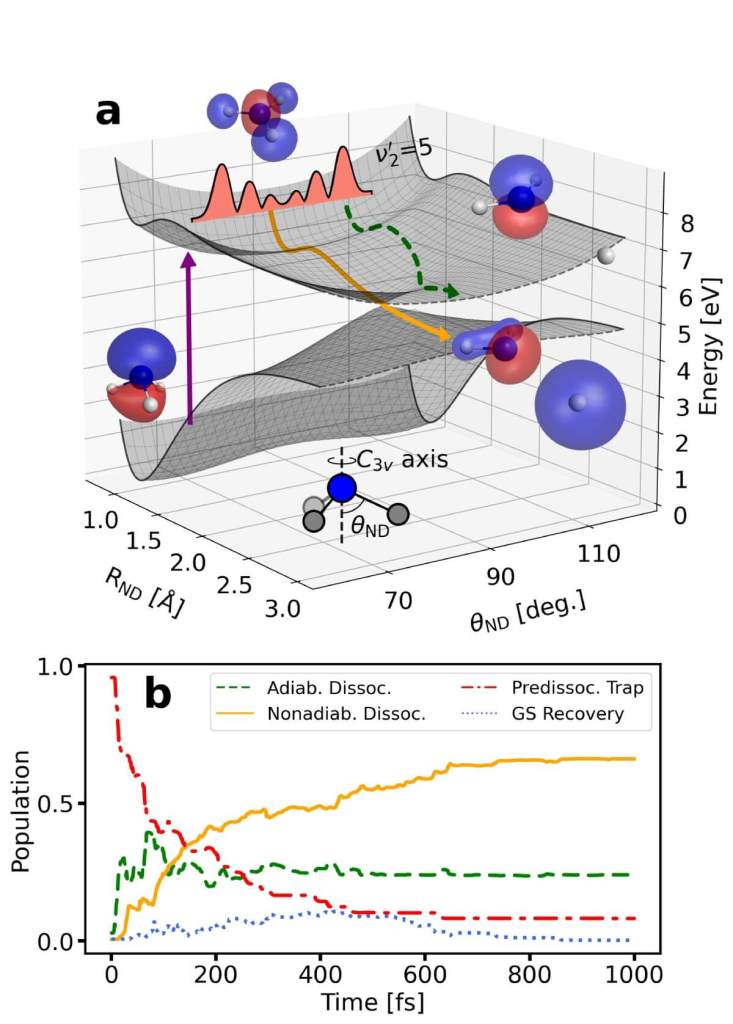
Para interpretar los datos experimentales, se utilizó un modelo de simulación cuántica conocido como AIMS, que permitió identificar cuatro canales de reacción distintos: predisociación atrapada, disociación adiabática, disociación no adiabática y recuperación del estado fundamental.
“Ver” un electrón significa mapear su presencia a través de su impacto en otros fenómenos físicos que sí podemos medir.
Los resultados mostraron que la señal de dispersión no podía explicarse únicamente por el movimiento de los núcleos atómicos, sino que requería la participación activa del electrón en el proceso. Las simulaciones mostraron que el electrón pasaba de un estado de tipo n3s (distribuido alrededor de la molécula) a un estado nσ* (más localizado), alterando por completo la imagen electrónica.
Este cambio fue confirmado al comparar dos modelos teóricos: uno que incluía el movimiento del electrón de valencia y otro que no. Solo el primero coincidía con los datos experimentales. “La contribución al patrón de dispersión se debe a la evolución de la distribución electrónica de valencia“.
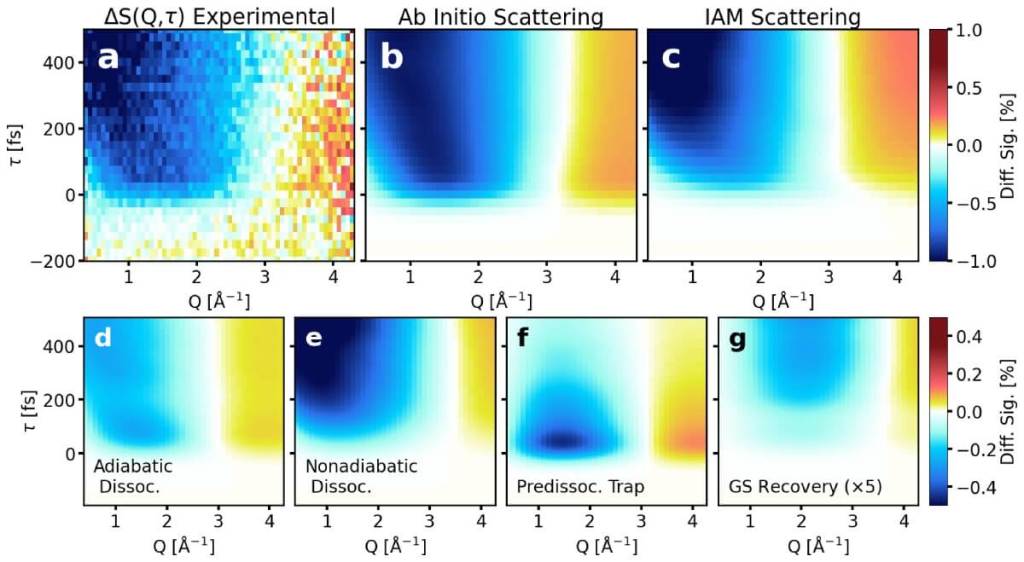
La química observada en tiempo real
Hasta este punto, la mayoría de los experimentos sobre reacciones químicas captaban estructuras fijas o cambios netos, sin poder seguir en detalle cómo un electrón se movía a lo largo de toda la reacción. Esta vez, la situación fue distinta: los investigadores consiguieron seguir el comportamiento electrónico desde la excitación inicial hasta la disociación completa de la molécula.
Para lograr esa resolución temporal, se utilizó el Linac Coherent Light Source (LCLS), una fuente de láser de electrones libres capaz de generar pulsos de rayos X de 35 femtosegundos. En combinación con un sistema de sincronización con resolución inferior a 15 femtosegundos, esto permitió registrar eventos que ocurren en escalas de tiempo menores que las vibraciones moleculares.
La calidad de los datos permitió incluso distinguir entre canales de disociación adiabáticos y no adiabáticos, es decir, si la reacción seguía o no el camino energético previsto. En uno de los modelos, el electrón permanecía delocalizado alrededor del radical ND₂, mientras que en el otro se relocalizaba cerca del centro de masa. Esta diferencia se reflejaba claramente en el patrón de dispersión recogido por los detectores.
Un paso hacia la química del futuro
Este avance tiene implicaciones directas para el desarrollo de nuevos materiales, fármacos o procesos industriales más eficientes. Comprender con este nivel de detalle cómo se comportan los electrones en plena reacción permite diseñar moléculas que respondan exactamente como se desea.
Según los investigadores, este experimento representa una referencia fundamental para futuras investigaciones. La posibilidad de combinar técnicas de dispersión ultrarrápida con simulaciones cuánticas avanzadas abre la puerta a estudiar reacciones más complejas, en moléculas con mayor número de electrones o en entornos tridimensionales más realistas.
Como señalan en las conclusiones, “anticipamos que los avances cercanos en técnicas de rayos X y esquemas de bombeo-sondeo permitirán estudiar el movimiento de un solo electrón en una amplia variedad de sistemas”. También cabe destacar que los nuevos desarrollos en pulsos de rayos X de attosegundos y esquemas de cronometraje subfemtosegundo podrían permitir seguir fenómenos aún más fugaces, como la migración de carga o la ionización por campos fuertes.
Más allá del electrón
El experimento con amoníaco es solo el primer paso de un camino mucho más ambicioso. Los autores ya trabajan en extender estas técnicas a moléculas más grandes y complejas, como las que forman parte de procesos biológicos fundamentales. Visualizar cómo se reconfigura la nube electrónica en proteínas o catalizadores podría revolucionar la forma de entender y diseñar nuevos sistemas químicos.
Por otra parte, los métodos empleados podrían integrarse con otras técnicas, como la espectroscopía ultrarrápida o la imagen por difracción de electrones, para obtener una imagen aún más rica y multidimensional del comportamiento cuántico de la materia.
La química, tal como se enseña y se modela, podría cambiar de manera sustancial en los próximos años si se logra integrar esta información en tiempo real. Ya no se tratará solo de saber qué productos se obtienen en una reacción, sino de ver cómo cada electrón decide, paso a paso, qué camino tomar.
Referencias
- an Gabalski, Alice Green, Philipp Lenzen, et al. Imaging valence electron rearrangement in a chemical reaction using hard X-ray scattering. Physical Review Letters, 2025. DOI: https://doi.org/10.1103/53h3-vykl.
Cortesía de Muy Interesante
Dejanos un comentario:

