Fuente de la imagen, Familia Chu
-
- Autor, Fergus Walsh
- Título del autor, Editor médico
-
Un niño de 3 años con una devastadora enfermedad asombra a los médicos con su progreso tras convertirse en la primera persona del mundo que recibe una innovadora terapia génica.
Oliver Chu padece una rara enfermedad hereditaria llamada síndrome de Hunter (MPSII), que causa daño progresivo al cuerpo y al cerebro.
En los casos más graves, los pacientes con esta enfermedad suelen morir antes de los 20 años. Sus efectos se describen a veces como un tipo de demencia infantil.
Antes del tratamiento, debido a un gen defectuoso Oliver no podía producir una enzima crucial para mantener las células sanas.
En una primicia mundial, el equipo médico del Hospital Real Infantil de Manchester, en Inglaterra, ha detenido la enfermedad alterando las células de Oliver mediante terapia génica.
El profesor Simon Jones, codirector del ensayo, declaró a la BBC: “Llevo 20 años esperando ver que un niño como Ollie esté mejorando tanto, y es realmente emocionante”.
En el centro de esta extraordinaria historia se encuentra Oliver, el primero de cinco niños en todo el mundo que recibieron el tratamiento, y la familia Chu, de California, que ha depositado su confianza en el equipo médico de Manchester.
Un año después de iniciar el tratamiento, Oliver parece desarrollarse con normalidad.
“Cada vez que hablamos de ello, me dan ganas de llorar porque es increíble”, dice su madre, Jingru.
La BBC siguió la historia de Oliver durante más de un año, incluyendo cómo los científicos de Reino Unido desarrollaron la pionera terapia génica y cómo el ensayo clínico que están llevando a cabo estuvo a punto de no materializarse por falta de fondos.
Conocimos a Oliver y a su padre, Ricky, en diciembre de 2024 en el centro de investigación clínica del Hospital Real Infantil de Manchester. Era un día importante.
Desde que le diagnosticaron el síndrome de Hunter en abril, la vida de Oliver, al igual que la de su hermano mayor, Skyler, quien también padece la enfermedad, ha estado marcada por las visitas al hospital.
Skyler había mostrado un desarrollo tardío del habla y la coordinación, pero inicialmente se atribuyó a haber nacido durante la pandemia.
Ricky me cuenta que el diagnóstico de sus hijos fue una completa sorpresa.
“Cuando te enteras del síndrome de Hunter, lo primero que te dice el médico es: ‘No busques información en internet porque encontrarás los peores casos y te desanimarás muchísimo'”.
“Pero, como cualquiera, lo investigas y piensas: ‘¡Dios mío! ¿Esto es lo que les va a pasar a mis dos hijos?'”.
Los niños nacen aparentemente sanos, pero alrededor de los dos años empiezan a mostrar síntomas de la enfermedad.
Estos varían y pueden incluir cambios en las características físicas, rigidez en las extremidades y baja estatura.
Puede causar daños en todo el cuerpo, incluyendo el corazón, el hígado, los huesos y las articulaciones, y en los casos más graves puede provocar deterioro mental grave y deterioro neurológico progresivo.
El síndrome de Hunter casi siempre se presenta en niños. Es extremadamente raro: afecta a uno de cada 100.000 varones nacidos en el mundo.
Hasta ahora, el único medicamento disponible para el síndrome de Hunter era Elaprase, que cuesta alrededor de US$400.000 por paciente al año y puede ralentizar los efectos físicos de la enfermedad.
El fármaco no puede atravesar la barrera hematoencefálica, por lo que no alivia los síntomas cognitivos.
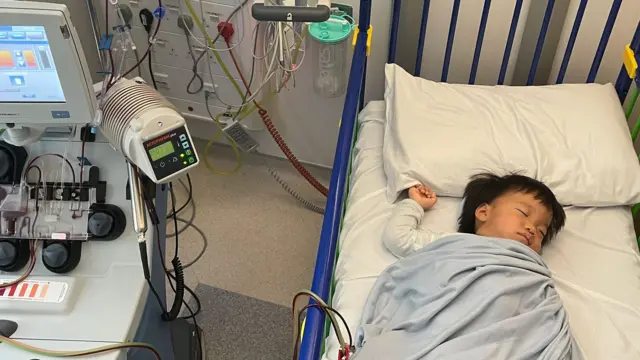
Pero hoy, Oliver está conectado a una máquina y se le están extrayendo células: el primer paso crucial para intentar detener su trastorno genético con este tratamiento único.
“Su sangre pasa por una máquina sofisticada que recolecta un tipo específico de células, las células madre, que se enviarán a un laboratorio para ser modificadas y luego se le administren de vuelta”, explica la Dra. Claire Horgan, especialista en hematología pediátrica.
La modificación de las células
Las células de Oliver se almacenan cuidadosamente y se envían a un laboratorio del Hospital Great Ormond Street (GOSH) de Londres.
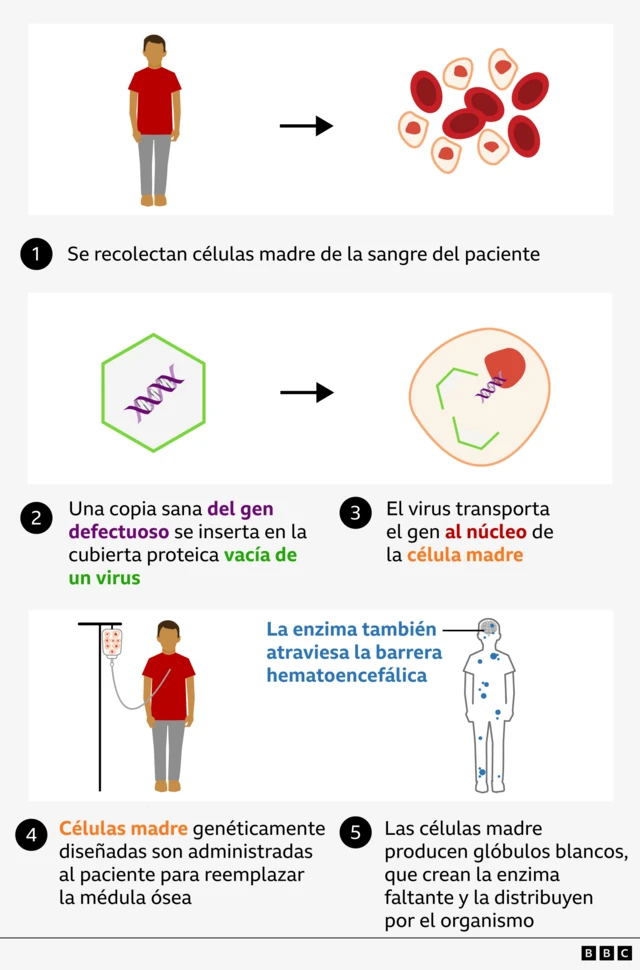
En el síndrome de Hunter, un error genético implica que las células carecen de las instrucciones para producir una enzima, la iduronato-2-sulfatasa (IDS), esencial para descomponer grandes moléculas de azúcar que con el tiempo se acumulan en tejidos y órganos.
Los científicos insertan el gen IDS faltante en un virus, al que se le extrae el material genético para que no pueda causar la enfermedad.
Un método similar se ha utilizado en otras terapias génicas, como el tratamiento de otra enfermedad hereditaria rara, la leucemia mieloide aguda (LMD).
La Dra. Karen Buckland, del Servicio de Terapia Celular y Génica del GOSH, explica: “Utilizamos la maquinaria del virus para insertar una copia sana del gen defectuoso en cada una de las células madre”.
“Cuando estas son inyectadas de vuelta a Oliver, deberían repoblar su médula ósea y comenzar a producir nuevos glóbulos blancos, y se espera que cada uno de estos empiece a producir la proteína [enzima] faltante en su cuerpo”.
Aún queda por resolver cómo introducir la enzima faltante en el cerebro.
Para solucionar esto, el gen insertado se modifica para que la enzima que produce cruce la barrera hematoencefálica con mayor eficiencia.
Día de infusión – febrero de 2025
Nos encontramos con Oliver de nuevo en el centro de investigación clínica del Hospital Real Infantil de Manchester.
Esta vez está con su madre, Jingru, mientras que Ricky se ha quedado en California para cuidar de Skyler.
Hay expectativa cuando un miembro del equipo de investigación abre un gran tanque metálico de criopreservación donde se congelan las células madre genéticamente modificadas de Oliver que fueron transportadas desde el GOSH.
Se extrae una pequeña bolsa de infusión transparente y se lleva lentamente a temperatura corporal en una bandeja con líquido.
Tras varias revisiones, una enfermera extrae el líquido transparente que contiene alrededor de 125 millones de células madre genéticamente modificadas con una jeringa.
Oliver está acostumbrado a los hospitales, pero se muestra inquieto y se retuerce mientras la enfermera le inyecta lentamente el tratamiento, aproximadamente una taza llena, en un catéter insertado en el pecho.
Jingru sostiene a Oliver firmemente en sus brazos. Después de 10 minutos, la infusión termina.
Una hora más tarde, se realiza una segunda infusión idéntica. Oliver sigue viendo dibujos animados en una pantalla portátil, ajeno a la posible importancia de lo que acaba de ocurrir.
Y eso es todo. La terapia génica ha terminado. Parece que todo concluyó bastante rápido, pero la ambición es enorme: detener de golpe la progresión de la enfermedad de Oliver con un tratamiento único.
Un par de días después, Oliver y Jingru regresan a California. Ahora, la familia y el equipo médico deben esperar para ver si la terapia génica ha funcionado.
Primeros indicios de progreso – mayo de 2025

En mayo, Oliver regresa a Manchester para unas pruebas cruciales para comprobar si la terapia génica está funcionando. Esta vez, toda la familia está aquí.
Nos encontramos en un parque del centro de Manchester y enseguida queda claro que las cosas van bien.
Oliver está más activo y curioso que nunca. Es cierto que ahora tiene libertad para jugar y ha salido del hospital, pero parece más radiante y sano.
Ricky está encantado: “Está muy bien. Hemos visto que ha progresado en el habla y la movilidad. En solo tres meses ha madurado”.
La gran noticia es que Oliver logró terminar la infusión semanal de la enzima faltante.
“Quiero pellizcarme cada vez que le digo a la gente que Oliver está produciendo sus propias enzimas”, dice Jingru. “Cada vez que hablamos de ello, me dan ganas de llorar porque es increíble”.
Me dice que se le ve “muy diferente” a antes del tratamiento, que habla “un montón” y que se relaciona más con otros niños.
Es muy agradable conocer finalmente a Skyler, de 5 años, quien es muy protector y cariñoso con su hermano menor.
“Mi deseo es que Skyler pueda recibir el mismo tratamiento”, señala Ricky. “Es como si Oliver hubiera tenido un cambio en su vida, y deseo lo mismo para Skyler, aunque sea un poco mayor”.
Inicialmente se pensó que Oliver era demasiado mayor para la prueba, ya que el tratamiento no puede revertir el daño existente, pero las pruebas demostraron que aún estaba prácticamente intacto.
Skyler parece disfrutar del mundo que lo rodea y se lo ve deseoso de tomarme de la mano y charlar mientras caminamos hacia el parque.
Ricky explica que Skyler tiene un retraso en el desarrollo del habla y la motricidad, pero que está recibiendo la terapia de infusión, que le permite recibir el tratamiento en su cuerpo, pero no en su cerebro.
“Eternamente agradecido”

Oliver regresa a Manchester cada tres meses para someterse a pruebas de seguimiento durante unos días.
A finales de agosto, nuevas pruebas confirman que la terapia génica está funcionando.
Oliver está claramente en plena forma y, hasta la fecha, ya han pasado nueve meses desde el tratamiento.
El profesor Jones, a quien Oliver llama Santa Claus por su barba blanca, está radiante: “Antes del trasplante, Ollie no producía ninguna enzima y ahora produce cientos de veces la cantidad normal”.
“Pero lo más importante es que vemos que está mejorando, que está aprendiendo, que tiene nuevas palabras y habilidades, y que se mueve con mucha más facilidad”.
Sin embargo, el profesor Jones se muestra cauteloso: “Debemos tener cuidado y no dejarnos llevar por la emoción, pero las cosas están tan bien como podrían estar en este momento”.
En el jardín de la azotea del hospital, Oliver juega con su padre.
“Es un niño completamente diferente. Corre por todas partes, no para de hablar”, dice Ricky.
“El futuro de Ollie parece muy prometedor y esperemos que esto signifique que más niños reciban el tratamiento”.
En total, se han inscrito cinco niños en el ensayo, procedentes de Estados Unidos, Europa y Australia. Ninguno es de Reino Unido, ya que los pacientes de aquí fueron diagnosticados demasiado tarde para ser elegibles.
Todos los niños serán monitoreados durante al menos dos años. Si el ensayo resulta exitoso, el hospital y la universidad esperan asociarse con otra empresa de biotecnología para obtener la licencia del tratamiento.
El profesor Jones afirma que el mismo enfoque de terapia génica se está aplicando a otros trastornos genéticos.
Hay tratamientos similares en ensayo en Manchester para la MPS tipo 1 o síndrome de Hurler y la MPS tipo 3 o síndrome de Sanfilippo.
Ricky y Jingru dicen estar “eternamente agradecidos” al equipo de Manchester por permitir que Oliver se uniera al ensayo.
Dicen estar asombrados por su progreso en los últimos meses. Oliver ahora produce la enzima que le faltaba y su cuerpo y cerebro están sanos.
“No quiero botar la sal, pero siento que ha ido muy, muy bien”, afirma Ricky.
“Su vida ya no está dominada por agujas y visitas al hospital. Su habla, agilidad y desarrollo cognitivo han mejorado drásticamente”.
“Ya no es solo una curva lenta y gradual a medida que crece, sino que ha mejorado exponencialmente desde el trasplante”.
El ensayo que casi no llegó a realizarse
Investigadores de la Universidad de Manchester, dirigidos por el profesor Brian Bigger, han dedicado más de 15 años a desarrollar la terapia génica para el síndrome de Hunter.
En 2020, la universidad anunció una colaboración con la pequeña empresa biotecnológica estadounidense Avrobio para llevar a cabo un ensayo clínico.
Pero tres años después, la empresa devolvió la licencia a la universidad después de que otro ensayo de terapia génica diera malos resultados y por la falta de fondos.
El primer ensayo en humanos, que pronto ayudaría a Oliver, estuvo en peligro incluso antes de comenzar.
El profesor Jones señala: “Tuvimos que actuar con mucha rapidez para intentar salvar la idea y encontrar otro patrocinador y otra fuente de financiación”.
Fue entonces cuando intervino LifeArc, una organización benéfica británica de investigación médica, aportando 2,5 millones de libras esterlinas (US$3,2 millones).
El Dr. Sam Barrell, director ejecutivo, declaró: “Un gran desafío para los más de 3,5 millones de personas en Reino Unido que viven con enfermedades raras es acceder a tratamientos eficaces; actualmente, el 95% de esas enfermedades no tienen uno”.
La familia Chu se siente aliviada de que el ensayo no se haya detenido y ahora espera que Skyler algún día pueda beneficiarse de la misma terapia génica que su hermano.
“Caminaría hasta el fin del mundo, de un lado a otro, cabeza abajo, descalzo, para asegurarme de que mis hijos tengan un futuro mejor”, afirma Ricky.
Información adicional: Nat Wright y Brijesh Patel

Suscríbete aquí a nuestro nuevo newsletter para recibir cada viernes una selección de nuestro mejor contenido de la semana.
Y recuerda que puedes recibir notificaciones en nuestra app. Descarga la última versión y actívalas.
Cortesía de BBC Noticias
Dejanos un comentario: